
Когнитивные нарушения отмечаются у 30–70% пациентов, перенесших инсульт [1,4–6]. Когнитивные нарушения могут быть легкими, умеренными и достигать степени деменции, вызывающей нарушение адаптации в профессиональной, общественной и бытовой сфере [5]. У пациентов, перенесших инсульт, легкие и умеренные когнитивные нарушения отмечаются примерно в половине случаев, деменция – в 10–20% случаев [1,4,6]. Постинсультные когнитивные нарушения обычно сочетаются с другой очаговой неврологической симптоматикой, вызванной инсультом.
В развитии постинсультных когнитивных расстройств может иметь значение не только перенесенный инсульт, но и предшествующее сосудистое поражение головного мозга («немые» инфаркты, лейкоареоз), сочетанное дегенеративное заболевание, например, болезнь Альцгеймера [1,4,6]. Поэтому возможность развития «чистых» форм постинсультной деменции, особенно после единичного инфаркта, ставится под сомнение, так как у пациентов с первым клинически значимым инсультом по данным нейровизуализации часто выявляются другие очаговые изменения белого вещества и подкорковых образований, а также атрофические изменения, характерные для нейродегенеративного процесса [1].
Когнитивные нарушения могут достигать степени деменции при инфаркте в стратегической для когнитивных функций зоне головного мозга (угловая извилина, зрительный бугор, хвостатое ядро, бледный шар, гиппокамп). Однако этот вариант когнитивных нарушений встречается относительно редко, его клиническая картина определяется локализацией поражения [1,6]. Например, при поражении доминантного зрительного бугра (обычно левого у правшeй), часто возникают брадифрения (снижение психической активности), дефицит внимания в сочетании с апатией, агнозией, апраксией и афазией.
Постинсультные когнитивные нарушения наиболее часто вызваны повторными (лакунарными и нелакунарными) инфарктами, многие из которых обнаруживаются только при нейровизуализации («немые» инфаркты головного мозга), и сочетанным поражением белого вещества головного мозга (лейкоареоз). Мультиинфарктная деменция (корковая, корково–подкорковая) представляет частый вариант постинсультной деменции [1,4,6]. У таких больных, помимо когнитивных нарушений, часто выявляются центральные парезы конечностей или рефлекторные изменения (оживление глубоких рефлексов, положительные рефлексы Бабинского, Россолимо). Атактические расстройства могут носить сенситивный, мозжечковый и вестибулярный характер, при деменции часто встречается апраксия ходьбы вследствие дисфункции лобных долей и разрыва корково–подкорковых связей. Для нарушений равновесия лобного генеза характерно замедление ходьбы, укорочение и неравномерность шага, затруднение в начале движений, неустойчивость при поворотах и увеличение площади опоры. Псевдобульбарный синдром проявляется рефлексами орального автоматизма, оживлением нижнечелюстного рефлекса, эпизодами насильственного плача или смеха, замедленностью психических процессов.
Нарушения памяти у больных, перенесших инсульт, представлены не столь выраженно, как при болезни Альцгеймера, и проявляются повышенной тормозимостью следов, замедлением и быстрой истощаемостью когнитивных процессов, нарушением процессов обобщения понятий, апатией [4–6]. Ведущими нарушениями могут быть замедленность мышления, трудности переключения внимания, снижение критики, понижение фона настроения и эмоциональная лабильность. Могут наблюдаться и первичные расстройства высших психических функций (апраксия, агнозия и т.д.), что наблюдается при локализации ишемических очагов в соответствующих отделах коры больших полушарий головного мозга.
Когнитивные нарушения могут возникать и вследствие внутримозгового кровоизлияния, при котором основным заболеванием часто является поражение мелких артерий, формирующееся на фоне длительной гипертонической болезни или амилоидной ангиопатии.
Диагноз постинсультных когнитивных нарушений основывается на клинических, неврологических и нейропсихологических данных, результатах магнитно–резонансной или компьютерной томографии головного мозга [4–6]. Для установления сосудистого характера когнитивных нарушений большую роль играет анамнез заболевания, наличие факторов риска цереброваскулярной патологии, характер течения заболевания, временная связь когнитивных расстройств и сосудистой патологии головного мозга. За последние десятилетия для диагностики сосудистой деменции было предложено несколько вариантов критериев диагноза. Одними из самых популярных критериев такого рода являются предложенные рабочей группой NINDS–AIREN в 1993 году критерии [11], согласно которым диагноз сосудистой деменции устанавливается в том случае, если у пациента одновременно выявляются деменция, признаки цереброваскулярного заболевания и между ними существует причинно–следственная взаимосвязь (развитие деменции в первые 3 месяца после инсульта).
Нейропсихологическое тестирование играет важную роль в диагностике синдрома сосудистых когнитивных нарушений. Краткая шкала оценки психического статуса (КШОПС), широко используемая для выявления когнитивной дисфункции, связанной с болезнью Альцгеймера, при когнитивных нарушениях сосудистой этиологии менее информативна и не может использоваться как метод выбора. Для выявления сосудистых когнитивных нарушений в качестве скрининговых нейропсихологических тестов (в дополнение к КШОПС) следует применять серию тестов для оценки лобной дисфункции, тест рисования часов [4,5].
Профилактика повторного инсульта
Важнейшее значение в ведении пациента, перенесшего инсульт и имеющего когнитивные нарушения, отводится вторичной профилактике инсульта, инфаркта миокарда и других сосудистых заболеваний [2,7,12].
Среди нелекарственных методов вторичной профилактики инсульта первостепенное значение имеют отказ от курения и злоупотребления алкоголем, регулярные физические нагрузки с учетом индивидуальных возможностей пациента, употребление в достаточном количестве свежих фруктов и овощей, растительного масла, свежей рыбы и ограничение потребления продуктов, богатых холестерином, и поваренной соли, снижение избыточного веса.
Нормализация артериального давления представляет собой одно из наиболее эффективных направлений вторичной профилактики инсульта, т.к. это снижает риск развития инсульта на 30–40% [7,12]. Выбор антигипертензивных средств проводится с учетом индивидуальных показаний, рекомендуется постепенное снижение повышенного артериального давления. Оптимальный уровень артериального давления, который следует достигнуть у больных, перенесших инсульт, окончательно не определен [7,12]. Если у больного нет выраженных стенозов или закупорок сонных артерий, следует стремиться к нормальному артериальному давлению (систолическое артериальное давление – 120–130 мм рт.ст., диастолическое артериальное давление – 80–85 мм рт.ст.). У больных, перенесших ишемический инсульт и имеющих гемодинамически значимый стеноз сонной артерии (особенно двусторонний) эффективность нормализации артериального давления остается сомнительной. В этих случаях необходима консультация сосудистого хирурга для решения вопроса о хирургическом лечении.
Больным, перенесшим ишемический инсульт, показаны антитромботические средства, статины и в части случаев реконструктивные операции на сонных артериях [1,7,12].
Статины являются одними из наиболее эффективных лекарственных средств для вторичной профилактики ишемического инсульта, особенно при наличии сочетанной ишемической болезни сердца, сахарного диабета, атеросклеротического поражения периферических артерий. Доказана эффективность аторвастатина в больших дозах (80 мг в сутки) у больных, перенесших некардиоэмболический инсульт. В настоящее время статины рекомендуются больным, перенесшим некардиоэмболический инсульт, а также больным с кардиоэмболическим инсультом при наличии других показаний [7].
Антитромботическая терапия показана всем больным, перенесшим ишемический инсульт. При кардиоэмболическом типе инсульта рекомендуются непрямые антикоагулянты, при некардиоэмболическом типе инсульта – антитромбоцитарные средства [1,7,12].
Применение непрямых антикоагулянтов рекомендуется больным с мерцательной аритмией, внутрижелудочковым тромбом, недавно (до трех месяцев) перенесенным инфарктом миокарда, ревматическим поражением митрального клапана, искусственным клапаном сердца и другой патологией, опасной повторением кардиоэмболического ишемического инсульта. Дозу варфарина подбирают постепенно, ориентируясь на международное нормализующее отношение, которое поддерживают на уровне 2–3.
При некардиоэмболическом типе инсульта рекомендуются антитромбоцитарные препараты: ацетилсалициловая кислота (АСК) (75–325 мг в сутки), клопидогрел (75 мг в стуки) или комбинация 200 мг дипиридамола медленного высвобождения и 25 мг АСК два раза в сутки. Прием антитромбоцитарных средств снижает риск развития повторного ишемического инсульта, инфаркта миокарда и острой сосудистой смерти в среднем на 20%. В Европейских рекомендациях по вторичной профилактике ишемического инсульта отмечается преимущество клопидогрела и комбинации 200 мг дипиридамола медленного высвобождения и 25 мг АСК над приемом одной АСК, поэтому их назначение вместо АСК рекомендуется во всех случаях, когда есть возможность длительного лечения этими лекарственными средствами [7]. Применение клопидогрела наиболее обосновано, когда больной, перенесший ишемический инсульт, имеет другие клинические проявления атеротромбоза: ишемическую болезнь сердца, артериальную недостаточность сосудов нижних конечностей.
Каротидная эндартерэктомия рекомендуется при выраженном стенозе (сужении 70–99% диаметра) сонной артерии на стороне перенесенного ишемического инсульта, сопровождающегося незначительной инвалидностью или без нее. Каротидную эндартерэктомию следует проводить только в специализированной клинике, в которой частота осложнений при этой операции не превышает 6%. Каротидную эндартерэктомию рекомендуется выполнить как можно быстрее после перенесенного ишемического события (оптимально в течение первых двух недель, но не позднее 6 месяцев с момента инсульта). При увеличении срока с момента ишемического поражения головного мозга эффективность каротидной эндартерэктомии постепенно снижается [7]. В тех случаях стеноза внутренней сонной артерии, когда каротидная эндартерэктомия противопоказана или стеноз расположен в недоступном для этой операции месте, можно использовать ангиопластику и установку стента. После установления стента рекомендуется в течение не менее одного месяца прием комбинации клопидогрела и АСК, в последующем прием одного из этих лекарственных средств [7,12].
Эффективность профилактики повторного ишемического инсульта значительно возрастает, когда у больного, перенесшего инсульт, используются все возможные эффективные лекарственные и нелекарственные средства.
Улучшение когнитивных функций
Для улучшения памяти и других когнитивных функций больным, перенесшим инсульт и имеющим когнитивные расстройства, рекомендуют посильную умственную нагрузку, тренировку памяти и лекарственные средства [4–6]. Большое значение имеет коррекция часто встречающихся у больных, перенесших инсульт, эмоциональных нарушений – депрессии и повышенной тревожности. Необходимо отменить или использовать в минимальных дозах лекарственные средства, ухудшающие когнитивные функции (средства с холинолитическим действием, анксиолитики, нейролептики, седативные средства).
Тренировка когнитивных функций (когнитивный тренинг) рекомендуется для улучшения и поддержки когнитивных возможностей пациентов, сохранения активного умственного уровня их повседневного функционирования. Положительные результаты когнитивного тренинга наиболее существенны при легкой и средней степени когнитивных нарушений. При проведении когнитивного тренинга необходимо опираться на сохранные когнитивные функции, целесообразно использование для тренировки привычных навыков, имеющихся интересов пациента.
При постинсультной деменции можно использовать ингибиторы ацетилхолинэстеразы (галантамин, донепезил, ривастигмин). Ингибиторы ацетилхолинэстеразы являются препаратами первого выбора в лечении болезни Альцгеймера, однако было доказано, что холинергический дефицит имеет место также и при сосудистой деменции [4,6,9]. Ингибиторы ацетилхолинэстеразы обладают способностью улучшать мозговой кровоток благодаря действию на сосуды или опосредованно через нейрональную активность. Наиболее изученными препаратами, показавшими хорошую эффективность при терапии сосудистой деменции, являются донепезил и галантамин.
Другим направлением нейротрансмиттерной терапии при постинсультной деменции является применение акатинол мемантина – антагониста NMDA–рецепторов к глутамату [5,9,10]. Повышение активности глутаматергической системы наблюдается как при нейродегенеративных заболеваниях, так и при сосудистых заболеваниях головного мозга. Глутамат является не только нейротрансмиттером, но нейротоксином. При различных по своей природе процессах, включая болезнь Альцгеймера и сосудистую деменцию, конечным этапом гибели клетки является эксайтотоксичность, обусловленная избыточным выбросом глутамата. Поэтому важной задачей становится коррекция обусловленных эксайтотоксичностью изменений при условии сохранности нормальной глутаматергической нейротрансмиссии. Действие акатинол мемантина основано на прямой селективной блокаде патологически возбужденных NMDA–рецепторов с уменьшением выраженности феномена эксайтотоксичности. Акатинол мемантин предохраняет нейроны от повреждения в условиях эксайтотоксичности и приводит к улучшению когнитивных функций больных.
При постинсультной деменции возможно и сочетанное применение ингибиторов ацетилхолинэстеразы и акатинол мемантина, поскольку данные препараты воздействуют на разные звенья патогенеза деменции, хотя не проводились исследования такой комбинации [9]. При выборе терапии следует также иметь в виду меньшее число побочных эффектов, связанных с применением мемантина, и его лучшую переносимость пожилыми пациентами в сравнении с ингибиторами центральной ацетилхолинэстеразы [9,10].
Для улучшения когнитивных функций у больных, перенесших инсульт, применяют пирацетам по 1,6–4,8 мг/сут., цитиколин по 1000–2000 мг в сутки, винпоцетин по 15–30 мг/сут., гинкго билоба по 120–160 мг/сут., церебролизин по 20–30 мл в/в на физиологическом растворе ежедневно в течение месяца, глиатилин по 1200 мг/сут. и другие лекарственные средства [1]. Вопрос об эффективности этих средств в отношении улучшения когнитивных функций остается не столь ясным, как использование ингибиторов центральной ацетилхолинэстеразы и акатинол мемантина. В настоящее время активно изучается эффективность применения этих средств у больных, перенесших инсульт и имеющих когнитивные нарушения.
Пирацетам представляет лекарственное средство, в отношении которого накоплен большой опыт в отношении его влияния на память и другие когнитивные функции как в экспериментальных, так и в клинических исследованиях [8,13,14]. В иностранной литературе на основании анализа результатов многоцентровых рандомизированных плацебо–контролируемых исследований отмечается, что ни одно из лекарственных средств не показало преимуществ в отношении улучшения каких–либо функций у пациентов, перенесших инсульт, однако при этом отмечаются положительные эффекты пирацетама, показанные в отношении речевых функций в некоторых плацебо-контролируемых исследованиях [8]. В последние годы в нашей стране широко используется препарат Омарон, представляющий комбинацию 400 мг пирацетама и 25 мг циннаризина.
Применение Омарона при умеренных постинсультных когнитивных
нарушениях
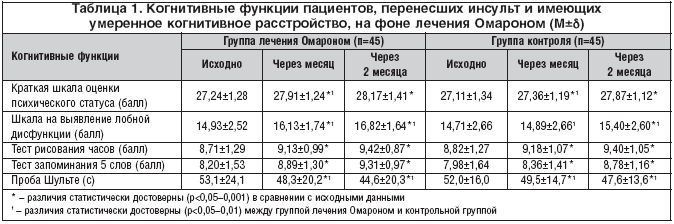
Нами проведено исследование эффективности и безопасности применения Омарона у больных, перенесших ишемический инсульт и имеющих умеренное когнитивное расстройство [3].
В исследование включено 90 пациентов, перенесших ишемический инсульт в сроки от одного до 12 месяцев и имеющих умеренное когнитивное расстройство. Методом рандомизации больные были разделены на две группы по 45 пациентов в каждой – группа лечения Омароном и контрольная группа. В контрольной группе 45 пациентов получали только базовую терапию (антигипертензивные, антитромбоцитарные стредства и другие лекарственные препараты) с целью профилактики повторного инсульта и других сердечно–сосудистых заболеваний. В группе лечения Омароном 45 пациентов в дополнение к базовой терапии получали Омарон по одной таблетке 3 раза в сутки в течение двух месяцев. Группы пациентов не различались по основным клиническим характеристикам (возраст, выраженность неврологических и когнитивных нарушений, степени инвалидности по шкале Ренкина).
За период наблюдения ни у одного из пациентов не развилось ни повторного инсульта, ни инфаркта миокарда или других сосудистых заболеваний. Проведение регулярной антигипертензивной терапии привело к нормализации артериального давления у большинства пациентов как в группе лечения Омароном, так и в контрольной группе без существенных различий между ними.
За два месяца наблюдения в обеих группах пациентов отмечено улучшение показателей неврологического статуса и уменьшение степени инвалидности, что в определенной степени могло быть проявлением естественного восстановления после перенесенного инсульта. В группе пациентов, принимавших Омарон, отмечена тенденция к более значительному восстановлению неврологических функций и уменьшению степени инвалидности.
При повторных обследованиях в группе лечения Омароном и в контрольной группе установлено достоверное улучшение показателей когнитивных функций по данным нейропсихологического исследования, что отражено в таблице 1. При этом в группе лечения Омароном отмечено достоверное улучшение когнитивных функций в сравнении с группой пациентов, получавших только базовую терапию.
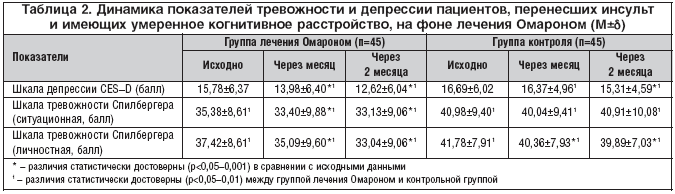
Через один и два месяца лечения в группе Омарона установлены достоверно более низкие показатели депрессии и тревожности, чем в контрольной группе, что отражено в таблице 2.
Результаты применения Омарона у пациентов, перенесших инсульт и имеющих умеренное когнитивное расстройство, показали хорошую переносимость лекарственного средства, отсутствие существенных побочных эффектов при его комбинации с антигипертензивными, антитромбоцитарными средствами и статинами, которые используются у пациентов с целью профилактики повторного инсульта и других сердечно–сосудистых заболеваний. У пациентов, принимающих Омарон, отмечено улучшение когнитивных функций по показателям нейропсихологических тестов уже через месяц лечения, и оно было еще более значительным через два месяца лечения. Положительная динамика когнитивных функций наблюдалась и у пациентов в контрольной группе, что в определенной степени могло быть связано с нормализацией у них артериального давления, спонтанным улучшением когнитивных функций и определенным опытом в решении нейропсихологических тестов. Через один и два месяца лечения выраженность депрессивных и тревожных расстройств была достоверно меньше в группе лечения Омароном, чем в контрольной группе. Улучшение эмоционального состояния пациентов могло положительно влиять на их когнитивные функции и быть одной из причин их улучшения. Положительный эффект пирацетама на когнитивные функции, опосредованный улучшением эмоционального состояния, отмечают и другие авторы [13,14].
Таким образом, применение препарата Омарон у пациентов, перенесших инсульт и имеющих умеренное когнитивное расстройство, показало его положительное влияние на когнитивные функции и эмоциональное состояние пациентов. Установлены хорошая переносимость Омарона, отсутствие существенных побочных эффектов при его комбинации с другими лекарственными средствами, которые используются для профилактики повторного инсульта и других сердечно–сосудистых заболеваний.
Литература
1. Вахнина Н.В., Никитина Л.Ю., Парфенов В.А., Яхно Н.Н. Постинсультные когнитивные нарушения // Журнал неврологии и психиатрии им. С.С. Корсакова Инсульт. Приложение к журналу, 2008, вып. 22, с. 16–21.
2. Дамулин И.В., Парфенов В.А., Скоромец А.А., Яхно Н.Н. Нарушения кровообращения в головном и спинном мозге // Болезни нервной системы: Руководство для врачей. Т.1 / Под ред. Н.Н. Яхно. — 4–е изд., перераб. и доп. — М.: ОАО «Издательство Медциина». — 2005. — С. 275 — 292.
3. Парфенов В.А., Беланина Г.Р., Вахнина Н.В. и др. Применение омарона у больных с умеренными постинсультными когнитивными нарушениями // Журнал неврологии и психиатрии им. С.С. Корсакова – 2009. – № 6
4. Преображенская И.С., Яхно Н.Н. Сосудистые когнитивные расстройства: клинические проявления, диагностика, лечение // Неврологический журнал — 2007. — Т.12. –№5. –С.45–50.
5. Яхно Н.Н. Когнитивные расстройства в неврологической практике// Неврологический журнал –2006. – Приложение № 1. – С.4–12.
6. Cerebrovascular disease, cognitive impairment and dementia. Second edition of Cerebrovascular disease and dementia. Edited by O’Brien J., Ames D., Gustafson L. Et al.–Martin Dunitz–2004.
7. European Stroke Organisation (ESO) Executive Committee; ESO Writing Committee. Guidelines for management of ischaemic stroke and transient ischaemic attack // Cerebrovasc Dis. – 2008; 25:457–507.
8. Flicker L, Grimley E.G Piracetam for dementia or cognitive impairment //Cochrane Database Syst Rev. 2001. – № 2. – :CD001011.
9. Kavirajan H., Schneider L.S. Efficacy and adverse effects of cholinesterase inhibitors and memantine in vascular dementia: a meta–analysis of randomised controlled trials. // Lancet Neurol. —2007. — Vol.6, N9. — p.782 — 792.
10. Orgogozo J.M., Rigaud A.S., Stoffler A. Efficacy and safety of memantine in patients with mild to moderate vascular dementia: a randomized, placebo–controlled trial (MMM 300). // Stroke. — 2002. — Vol.33, N7. — p.1834 — 1839.
11. Roman GC, Tatemichi TK, Erkinjuntti T. et al. Vascular dementia: diagnostic criteria for research studies. Report of the NINDS–AIREN International Workshop // Neurology. — 1993. — Vol.43, N2. — p.250 — 260.
12. Sacco R. L., Adams R., Albers G. et al. Guidelines for Prevention of Stroke in Patients With Ischemic Stroke or Transient Ischemic Attack: A Statement for Healthcare Professionals From the American Heart Association/American Stroke Association Council on Stroke: Co–Sponsored by the Council on Cardiovascular Radiology and Intervention: The American Academy of Neurology affirms the value of this guideline // Stroke – 2006; 37: 577 – 617.
13. Tariska P., Paksy A Cognitive enhancement effect of piracetam in patients with mild cognitive impairment and dementia // Orv Hetil. 2000. – Vol.141. –: P. 1189–1193.
14. Winblad B. Piracetam: a review of pharmacological properties and clinical uses // CNS Drug Rev. 2005. – Vol. 11. – P.169–182.
Парфенов В.А.
по материалам РМЖ

 Опубликовано в категории:
Опубликовано в категории:  Метки:
Метки: